 发病机制
发病机制
发病机制:
糖尿病视网膜病变的发病机制迄今还不完全明了。从临床过程和多数研究结果,本病历来被认为主要是源于视网膜血管,尤其是微血管系统的损害,随后引起视网膜一系列的病理改变。
糖尿病的糖代谢机制紊乱是产生糖尿病性视网膜病变的根本原因。醛糖还原酶在葡萄糖高浓度下转化为山梨醇再成为果糖,并使半乳糖转化为卫茅醇。由于山梨醇和卫茅醇在细胞内很少进一步发生代谢,并因其极性而难于透出细胞膜,细胞内浓度增大致渗透压升高,水分渗入细胞引起电解质失衡和代谢紊乱。晶状体上皮细胞即含有高浓度醛糖还原酶,故
半乳糖血症和
糖尿病实验动物易发生白内障。视网膜毛细血管周细胞在
糖尿病患者发生的选择性丧失,也与含有较多的醛糖还原酶有关。由于周细胞损害和消失,减低了毛细血管的收缩力和调节毛细血管内血流量的作用。
糖尿病患者血小板的黏着和凝集异常,以及血液成分改变和黏度增高等,都可能与视网膜的循环障碍和缺血有关。据检测发现血小板的凝集功能随
糖尿病视网膜病变的发生和发展有不断加强的趋势。并且与生长激素水平增高导致血中第Ⅷ因子水平上升有较大关系。第Ⅷ因子由血管内皮分泌,与红细胞凝集有关,还可促进血小板的集结和黏附作用。在血小板黏附于血管内皮细胞过程中,细胞壁中的磷脂物转化为凝栓质A
2(或称血栓素A
2),可使血管收缩并进一步使血小板凝聚。这些异常的血小板黏着和凝聚便可能是引起毛细血管闭塞的重要因素,以至造成视网膜组织缺血缺氧,成为
糖尿病视网膜发生病变的主要原因。
有些
糖尿病患者的血液黏度增高,尤其是那些
糖尿病控制不良与血管并发症较重者更为明显。红细胞凝集性增加和变形能力降低,便不能穿过管径细小的毛细血管;加上血浆蛋白,如纤维蛋白原和α球蛋白等含量升高,都使血液黏滞度加大,导致血管内皮损害,造成血管堵塞,易致微血栓生成。
糖尿病视网膜病变的严重程度与这些因素有一定的关系。
关于生长激素在
糖尿病视网膜病变中所起的作用,曾有作者发现女性
糖尿病患者产后发生出血性垂体坏死(Sheeham综合征)后,严重的
糖尿病视网膜病变病情随即逆转。近年有人对一些患有
糖尿病的侏儒患者作过10年以上的随访观察,未发现他们发生糖尿病性视网膜病变。据认为生长激素分泌增高可抑制糖代谢,导致细胞内山梨醇积聚,增加
糖尿病血管中糖蛋白和黏多糖的沉积并加速血管硬化,促进视网膜微血管微
血栓形成而引起视网膜病变。
至于
糖尿病视网膜病变的新生血管增殖性病变,与体内许多产生新生血管的疾病相仿,属于一种代偿机制,由于组织缺氧的诱导,出现一种可弥散的“血管增殖因子”。曾经分离出一种新生血管生长因子的化学物质,但其性质尚不十分明了。用全视网膜光凝治疗,使
糖尿病视网膜病变的眼底和虹膜上的新生血管消退,也间接说明确有这种可弥散的因子存在。
此外,有一些研究表明不同类型的
糖尿病患者具有不同遗传基础,在免疫遗传学的观察研究中,不同类型HLA抗原与特定的
糖尿病视网膜病变类型的发生率有较密切的关系。
糖尿病累及视网膜是先有视网膜组织代谢的损害,然后才是组织学或检眼镜下可见的血管异常。视网膜神经元功能异常出现最早,表现在视网膜电图的震荡电位参数的改变。但这种观点的确立还需要更多的观察研究和佐证。
早期
糖尿病视网膜病变除微动脉瘤以外,还有不同程度的视网膜静脉扩张,尤其是小静脉,常呈环绊状等不规则形状。在内核层或外网状层内常有毛细血管或微动脉瘤破裂出血,早期较少神经纤维层出血。病程较长和较重的视网膜病变,血-视网膜屏障破坏,液体渗漏入视网膜,发生视网膜水肿和硬性渗出。外网状层在水肿时最为明显,其他各层因以神经轴突和广泛的细胞成分为主,故含水较少。黄斑部视网膜有较多放射状排列的Henle纤维,也常有较重的水肿。硬性渗出则是血管渗漏的液体和脂质沉积于外网状层,液体成分逐渐吸收以后遗留的蜡黄色斑块。
在
糖尿病视网膜病变长期持续的进程中,视网膜毛细血管闭塞,导致神经纤维层的灶性梗死,成为白色絮状的软性渗出。与此同时这一阶段先后发生的视网膜无灌注区则在荧光血管造影图上可明确显示。上述缺血缺氧严重,血管损害不断加剧的视网膜病变诱发的新生血管,可从静脉发起,或源于一簇细小的视网膜内微血管异常。新生血管的内皮细胞有窗样改变,并且细胞间没有紧密连接,故荧光血管造影时有特征性的大量迅速渗漏荧光。推测视盘上缺乏真正的内界膜限制,可能与这一部位较多出现新生血管有关。新生血管也常沿脱离的后玻璃体表面已发生的结缔组织生长。一般新发的新生血管为裸露而无结缔组织成分,以后逐渐伴发视网膜玻璃体结缔组织增生,玻璃体膜增厚。长期存在的新生血管渐渐发生退行改变,最后在长时间的自然病程中可自行萎缩。
 临床表现
临床表现
临床表现:多数
糖尿病视网膜病变患者有
糖尿病的多饮、多尿、多食和疲乏、消瘦等症状。在视网膜病变初期,一般无眼部自觉症状。病变发展,可引起不同程度的视力障碍。若黄斑区受累,可有视野中央暗影,中心视力下降和(或)视物变形等症状。视网膜小血管破裂,少量出血入玻璃体,患者可自觉眼前有黑影飘动。当新生血管大量出血到玻璃体腔,视力可严重丧失,仅存光感。黄斑区以外的视网膜血管闭塞,或增殖性视网膜病变导致
视网膜脱离,则视野出现相应部位较大面积的缺损。
糖尿病视网膜病变的临床体征多种多样。
在
糖尿病视网膜病变的自然病程中,早期即有视网膜血管自我调节机制的紊乱和血流变异常,以及血-视网膜屏障破坏。临床上在视网膜病变早期最先出现视网膜微
血管瘤,以后逐渐出现视网膜静脉和动脉的较大血管的病变,并有血管外的出血和渗出等视网膜组织损害。
1.血管病变
(1)毛细血管异常:
①微
血管瘤:微动脉瘤是检眼镜和荧光血管造影能查见的最早的
糖尿病视网膜病变。这种改变虽可见于其他疾病,如高血压或
视网膜静脉阻塞等视网膜的病变,但以
糖尿病视网膜病变发生的频率最高,数量也最多,颇具有特征性。微动脉瘤在检眼镜下表现为视网膜上的红色小点,常呈圆形,颜色深红类似视网膜深层的小出血点。若对视网膜上出现的红色小点不能分辨为微动脉瘤或小出血点,则可在随访观察中注意,后者常在较短期内消退。
糖尿病视网膜病变的微动脉瘤常先出现在眼底后极部,尤其在黄斑区,并多在颞侧。随病程延长,则分布于视网膜各处并常密集成群。微动脉瘤有时在视网膜与异常扩张的微血管相连,并常位于毛细血管闭塞区周围。微动脉瘤的半衰期约数月,逐渐发生内皮结构破坏和透明变性并瘤腔闭塞。在视网膜病变进程中,新的微动脉瘤发生与旧的消失,在视网膜各处交替发生。
眼底荧光血管造影可见微动脉瘤表现为周界清晰的圆的小荧光点,大小为20~30µm,从荧光血管造影发现微动脉瘤在视网膜微循环的动静脉两侧均有分布。多数在检眼镜下不易或不能查见的微动脉瘤,荧光血管造影检查能使其清楚的显现而确诊。如瘤腔被血球充填栓塞,则不能显荧光,检眼镜检查也常不能与小出血点鉴别。
视网膜缺氧是微动脉瘤形成的主要因素,据推断可能与新生血管形成的机制有关或类似,但程度较轻,或许是新生血管形成的一种夭折现象。微动脉瘤通常先见于视网膜内核层,逐渐扩散至内网状层,其内皮结构不建全,如瘤腔未栓塞则血中蛋白、其他物质和荧光素分子均可渗出到视网膜内,
血管瘤较多时漏出物增多,导致其周围视网膜不同程度的水肿,是造成视网膜水肿的一个重要原因。
②毛细血管扩张和渗漏:视网膜毛细血管管径为5~12µm,荧光眼底血管造影检查可显示微细的血管网。黄斑区毛细血管丰富致密,但朝向黄斑中心部分迅速变细而且稀疏,在中心凹周围形成环形的连续网络,称为黄斑区的毛细血管拱环。毛细血管扩张也是一种
糖尿病患者视网膜的早期改变。
糖尿病人在检眼镜检查未发现视网膜病变以前,部分患者经荧光血管造影,发现视网膜毛细血管的能见度增强,表明有轻度毛细血管扩张,可能是由于代谢需要的循环自我调节机制紊乱,这是一种可逆的微循环功能性改变。随病程进展,组织缺血缺氧的程度加重,自动调节不能代偿,毛细血管便发生器质性损害。在较严重的
糖尿病视网膜病变,可出现毛细血管明显的异常扩张,粗细不匀和迂回扭曲,可呈U字形弯曲或其他奇特形态。统称为视网膜内微血管异常。黄斑区病变较重者,可在荧光血管造影片上查见黄斑毛细血管拱环变形,甚至拱环毛细血管网络破坏而不连续。
扩张的毛细血管和微
血管瘤,管壁通透性异常,在荧光血管造影图上表现为初期荧光渗漏渐向四面弥散,后期成为边界模糊的荧光斑团。这种血浆物质的外渗是视网膜渗出、出血和水肿等病变的基础。有些较重的
糖尿病视网膜病变可见视神经盘周围辐射状毛细血管扩张和荧光渗漏,造影后期视盘边界和血管轮廓模糊,其周围组织有荧光着染。这些现象常预示有发展成为增殖性视网膜病变的可能。
③毛细血管无灌注区:这也是惟有眼底荧光血管造影检查才能发现的较严重和有重要意义的视网膜病变。这个体征说明毛细血管管壁细胞破坏并有较严重的小血管闭塞。在造影图上表现为大小的斑点状或片状无荧光的暗区,此区周围的毛细血管正常形态中断。无灌注区多先发生于眼底赤道部视网膜,渐向后极和周边发展。无灌注区累及一整个微循环单位,即由供养小动脉、属于它的毛细血管网和收集小静脉所供应的范围。在无灌注区内常见微
血管瘤、或微
血管瘤链和异常扩张的微血管。
无灌注区在视野中表现为相应位置的暗区,虽然往往因其缓慢发生且位置未在眼底后极正中而不引起明显自觉症状。无灌注区波及黄斑区者,在荧光血管造影图上表现为中心凹的无血管区比正常增宽。若中心凹周围毛细血管拱环的连续性破坏,则造成黄斑缺血性损害,视力的预后不良;视盘黄斑束的部位出现无灌注区者,视力损害也很严重。
④动静脉交通:检眼镜检查有时可见比毛细血管粗大,将动静脉直接连接的异常扩张的血管。造影检查时,这些血管多数可有管壁荧光着色和较轻微的渗漏,并位于毛细血管闭塞区内。这种血管多系毛细血管闭塞过程中发生的侧支,是视网膜血管床中试图恢复正常血流的一种表现。
(2)视网膜动、静脉异常:
①视网膜小动、静脉异常:有一些视网膜的小动、静脉血管异常用检眼镜不易发现,但在荧光血管造影时显而易见。这些小血管分支的起源处变狭窄,而其远端部分则扩张,管壁有荧光着染和渗漏使血管轮廓变得模糊。在更重的病例,则小血管管腔闭塞,在分支处遗留有短棍状血管残端。上述血管改变多出现在较重的视网膜病变,并常位于毛细血管闭塞区的边缘,有些小血管还表现为串珠状曲张,或呈环形弯曲,有时还见有血管鞘包绕。
②视网膜大动、静脉异常:
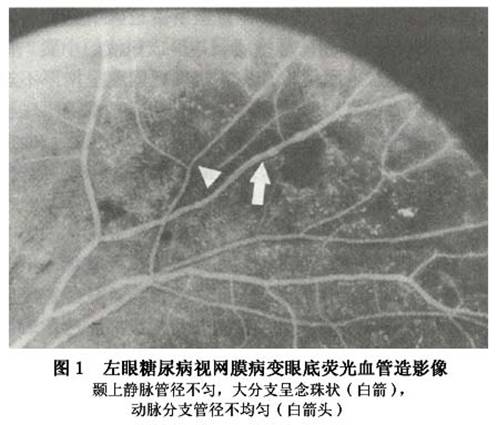
糖尿病视网膜病变最常表现静脉迂曲扩张和管径不匀,在其他特征性改变尚不明显时已可查见。视网膜病变后期更为突出,静脉血管可呈典型的串珠状或腊肠状(图1),血管可盘绕成环形,有的并有白鞘。视网膜病变严重者,静脉管壁有荧光着染和滞留,并现荧光渗漏。有时还可发生分支静脉阻塞。
视网膜上大的动脉血管异常在检眼镜下常不显著,但荧光血管造影常可显示有管径粗细不匀,有节段性的扩张和狭窄。在造影后期,其异常节段表现为荧光着色和渗漏,与静脉的表现类似,并常与静脉改变相伴出现。这些改变在有血管闭塞的部位尤为明显。
2.血管外损害
(1)
糖尿病患者视网膜出血位置较深,常在内核层,常呈圆形斑点状,多与视网膜微动脉瘤或微血管异常相伴发生,很少是不伴有其他血管异常的单纯出血。神经纤维层火焰状出血在伴有高血压的患者中较多见。各种出血斑常与棉絮状渗出斑邻近或与其重叠。荧光血管造影图上,出血斑点表现为遮蔽背景荧光的黑色斑点,在这些出血斑的暗影内或其边缘,常现微动脉瘤群集或呈链状分布的荧光点。视网膜出血严重者可融合成大片累及视网膜各层,甚至突破内界膜成视网膜前出血,表现为上界呈水平线,下界呈半球弧形的舟状出血团。如果大量出血再突破玻璃体膜进入玻璃体腔内,则引起玻璃体混浊,导致重度视力障碍。
(2)渗出:
①硬性渗出:
糖尿病视网膜病变较早期常在眼底后极部出现边界比较清楚的蜡黄色点片状渗出,称为硬性渗出。这种渗出大小不等,可以在黄斑区或其附近,呈环状。硬性渗出位于视网膜深部的外网状层,主要是视网膜毛细血管渗漏物逐渐吸收以后遗留的脂质。这种脂质组成的黄白色渗出物可渐被吸收而消散,另外又出现新的硬性渗出。眼底荧光血管造影检查在这些渗出斑的边缘或环形渗出的中央常见明显的毛细血管异常和渗漏,并在这些渗出吸收以后遗留的瘢痕处显现强荧光,表明该处有毛细血管和色素上皮的损害。
②棉絮状斑――软性渗出:棉絮状斑为大小不等、形状不规则的灰白或乳脂色调的视网膜渗出斑,边界模糊,呈棉絮或绒毛样,位于视网膜浅部的神经纤维层。常出现于眼底后极部视网膜距视盘3~4个视盘直径的范围内,多数沿大血管附近分布。这种渗出斑是视网膜微血管闭塞性损害,组织严重缺血以致神经纤维层发生梗死的表现。因此,软性渗出显示视网膜循环重度障碍引起的组织破坏,预示视网膜病变有迅速发展成为增殖性改变的趋势。软性渗出的半衰期为半年至1年半,年龄较大的患者消散较缓慢。
由于这种渗出附近多有微动脉瘤和微血管异常的渗漏,荧光血管造影时这种渗出斑常有荧光着染。
3.黄斑病变
糖尿病视网膜病变的各种黄斑病理改变,包括出血、渗出水肿和微
血管瘤等,是严重影响视力的重要原因,其中以黄斑水肿最常见。多数较轻的黄斑水肿在检眼镜下不易鉴别,重度黄斑水肿在单纯性视网膜病变后期和增殖性视网膜病变都可以发生。视网膜毛细血管通透性改变,渗漏液体蓄积于黄斑区中心凹周围呈辐射状排列的Henle纤维之间,形成积液的小囊。重度
黄斑囊样水肿检眼镜检查见黄斑区视网膜呈增厚不透明外观,中心凹表现蜂窝状隆起。裂隙灯显微镜眼底检查发现该处视网膜肿胀变厚可达正常的2~3倍。长期持续的
黄斑囊样水肿可成为永久性囊样变性甚至视网膜穿孔,致不可逆的视力丧失。
有黄斑水肿的眼底,荧光血管造影常见黄斑区毛细血管闭塞,中心凹周围黄斑毛细血管拱环破坏。早期较轻的水肿和拱环不完整,并不影响视力,只是黄斑区毛细血管和微
血管瘤通透性增大有荧光渗漏,造影后期在黄斑区呈模糊的斑片状荧光。重度的
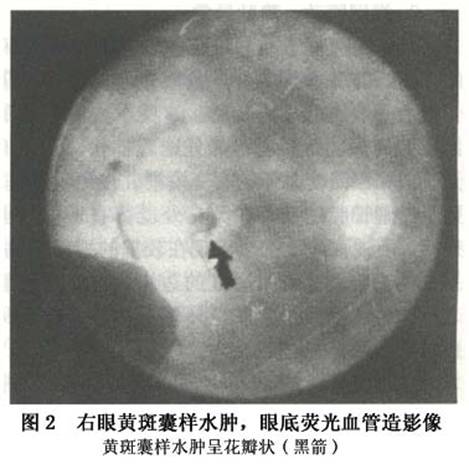
黄斑囊样水肿,黄斑区荧光渗漏显著,造影后期呈围绕中心凹排列、呈现有分隔的花瓣状或卵石状囊样荧光形态(图2)。
4.增殖性病变
糖尿病视网膜病变进展到一定程度,血管病变加剧,视网膜组织重度缺血缺氧,视网膜血管壁萌发新生血管。这些新生血管好发于视盘及其附近,或近赤道区的视网膜中央动静脉血管。初期较细小的新生血管有的用检眼镜不易察明,但因其管壁异常,大量渗漏荧光素,经眼底荧光血管造影而易于识别。新生血管位于视网膜表面,多数突出于内界膜之外而与玻璃体接触。明显的新生血管在检眼镜下表现为视网膜大血管邻近蜷曲迂回的细血管网。新生血管管壁结构不健全,易于出血,出血较多时往往穿入玻璃体内,严重妨碍视力。
与新生血管出现的同时,视网膜组织在新生血管附近逐渐发生纤维细胞增殖,形成纤维条带。这种在视网膜表面和邻接玻璃体处发生的血管纤维性增殖,称为
增殖性玻璃体视网膜病变。这些增殖带随病程延长而增多,并收缩牵引而引起新生血管出血或
视网膜脱离等不良后果。但也有少数病例,经过漫长的病程,新生血管萎缩闭塞,未发生大量出血或
视网膜脱离可幸存一定的视力。
5.分期
糖尿病视网膜病变的临床眼底表现形态多样,为了明确诊断,观察病情演变,衡量治疗效果和估计预后,并在临床和研究工作中对病变作准确的记录和描述,曾有不少国内外作者对
糖尿病视网膜病变进行过多种不同的分型和分期。归纳起来,都以是否出现视网膜新生血管为标志,分为没有发生新生血管的背景型(或单纯型)和出现新生血管以后的增殖型,这是多数一致的观点。其余具体分期的标准,内容虽大同小异,但极不统一。我国1984年6月在哈尔滨举行第1次全国眼底病学术讨论会时,根据
糖尿病视网膜病变的系列临床表现特征和病理改变过程,参考各地
糖尿病视网膜病的研究成果,以及历来的分期方法,制订了“
糖尿病视网膜病变临床分期标准”(表1),经同年10月在南宁召开的中华医学会眼科学会第三届全国学术会议讨论通过并公布实行。在我国临床的医疗和研究工作中对
糖尿病视网膜病变的分型分期有了规范和统一的标准。
没有新生血管形成的
糖尿病视网膜病变称为单纯型病变,即过去沿用过的国外翻译名称背景性视网膜病变。这一时期的病变局限在视网膜内。单纯型病变的早期,虽然用玻璃体荧光光度测定的方法可在没有任何眼底体征以前测知视网膜血管或血-视网膜屏障可能发生的破坏,但视网膜微动脉瘤和(或)小出血点仍然是最早出现并比较确切的视网膜病变的体征。带黄白色的蜡样硬性渗出斑点,说明血管系统功能异常,通透性增大,血液成分逸出。而白色软性渗出则表示微循环重度紊乱,血管破坏严重,视网膜神经纤维层发生梗死。在这个阶段并有多处局灶性或广泛的视网膜无灌注,常预示即将发生新生血管,故又称为
糖尿病视网膜病变的增殖前期。至于视网膜病变的增殖期,即在视网膜循环对组织缺氧不能代偿的情况下,从发生新生血管开始。新生血管从视网膜表层突破内界膜,位于视网膜和玻璃体之间的间隙。后期纤维增殖增多,血管纤维增殖穿越玻璃体膜进入玻璃体内。增殖组织或玻璃体的收缩都可引起
视网膜脱离或
玻璃体积血而严重影响视力。
上列
糖尿病视网膜病变分期标准,重点突出疾病演变中能体现病变实质的主要眼底表现特征,比较准确、合理地反映
糖尿病视网膜病变的临床和病理进展和变化过程,还对单纯型视网膜病变中各期病情轻重程度的概念,结合临床表现作了适当的数量表达。这个标准比较简明扼要,便于在各级医疗卫生单位的医疗、科研和教学中应用。但这一
糖尿病视网膜病变分期标准是根据检眼镜观察眼底体征设计,没有包括在检眼镜下可能不易察见、并与视网膜大部分病变发生的时期规律不完全一致的黄斑病变的分期。为适应20世纪80年代初,国内眼底荧光素血管造影技术和视网膜病变激光治疗技术还远未开展的初起阶段,这一诊断标准在我国临床医疗和眼病普查等广泛应用中起到统一规范的作用。在迄今近20年中,眼底荧光血管造影包括荧光素与吲哚青绿造影的诊断方法以及眼底疾病激光治疗应用已在国内广泛开展和逐渐普及,对检眼镜下不能完全发现的
糖尿病视网膜病变的微动脉瘤、视网膜内微血管异常、视网膜无灌注区、视网膜新生血管以及
糖尿病黄斑病变等的诊断和治疗发挥了很大的优势,在临床和研究中起到很重要的作用。譬如影响视力较重的
糖尿病性黄斑病变,早期体征在检眼镜下多不明显,而荧光素血管造影检查常显示黄斑区荧光素渗漏,对病变的组织结构和病变严重程度等还可通过造影的时相与影像特征表现透彻了解,从而对激光治疗的指征和方法等起重要作用。此外,
糖尿病性黄斑病变的发生发展与黄斑区外大部分视网膜病变发生的轻重程度与时期早晚的规律并不完全一致。有为数不少的
糖尿病视网膜病变的患眼并不出现黄斑病变,有一些早期
糖尿病视网膜病变患眼可发生较重的弥漫性黄斑水肿,也有
糖尿病视网膜病变晚期的患眼出现轻度的局限性黄斑水肿者。因此视网膜上这一中央部分在生长发育与组织结构有一定独特性能的黄斑区,在
糖尿病视网膜病变中发生黄斑病变的特定性分型和分期标准也必须适应其独具的特征。1984年Sigelman提出按黄斑病变轻重不同的分期标准为多数学者接纳和采用,其主要内容如下:第1期,背景性
糖尿病黄斑病变。眼底荧光素血管造影检查发现视网膜有范围较小和数目较少的缺血灶;晚期黄斑区有轻微荧光素渗漏。第2期,局限性渗漏性黄斑病变,黄斑区有不等程度的硬性渗出斑,眼底荧光素血管造影显示黄斑周围有较多缺血灶,后期有来自微动脉瘤和扩张毛细血管的较强荧光素渗漏。第3期,弥漫性渗漏性黄斑病变,检眼镜下有明显弥漫性黄斑水肿,有多量硬性渗出物或形成渗出环;眼底荧光素血管造影显示黄斑区及其周围视网膜有多处缺血灶,晚期有弥漫性荧光素渗漏,并形成黄斑区微囊样荧光素积存。第4期,囊性退变性黄斑病变,眼底荧光素血管造影显示眼底后极有广泛的视网膜缺血灶和强荧光素渗漏,晚期有以黄斑中心凹为中心的花瓣状荧光素积存。
 治疗
治疗
治疗:糖尿病视网膜病变的治疗,原则上应经常将高血糖控制在正常水平。虽然由于发病机制比较复杂与病变类型的差异,但若糖尿病患者高血糖和周身病情得到长期的较好控制,对延缓其视网膜病变的进行和减轻病情有肯定的效果。这种状况多半与患者高血糖即血中糖化血红蛋白与氧的亲和力增强且不易释放的机制有关;若长期使血糖控制在正常水平,对缓解视网膜缺氧有一定的作用。
对于糖尿病视网膜病变的治疗,一般说来,针对具体病情,可分3个方面概述如下:
1.药物治疗 对糖尿病视网膜病变还缺乏特效的药物治疗。20世纪60年代初期发现经
水杨酸盐治疗类风湿关节炎同时有糖尿病的患者,糖尿病视网膜病变的发生率极低。阿司匹林对血小板凝集有抑制作用,在临床上并对微循环血栓形成的预防有一定帮助。基于这些临床和理论上的认识,近年对糖尿病患者曾经应用阿司匹林口服300mg,1次/d,预防视网膜病变的发生,或在早期糖尿病视网膜病变时服用,可能有一定的作用。
对于视网膜黄斑区及其周围有环形硬性渗出及血脂偏高的糖尿病患者,应摄取低脂膳食,服用降胆固醇药
安妥明250mg,4次/d,曾有报道可减少视网膜渗出和起到增进视力的效果。此外可口服药物
导升明(doxium),化学名为2,5-
二羟基苯磺酸钙,用于早期糖尿病视网膜病变,有可能减轻糖尿病视网膜毛细血管的易渗漏性,降低血的高黏稠度和血小板的凝聚力,达到减轻糖尿病视网膜病变的目的。
2.手术治疗 手术疗法主要用于治疗增殖性视网膜病变的并发症,如新生血管引起的玻璃体积血,视网膜玻璃体增殖条带引起的牵拉性视网膜脱离和孔源性视网膜脱离等。若玻璃体积血严重且较长时间不能消散吸收,采用玻璃体切除手术,以达到清除积血,切断和分离机化条膜,缓解对眼底组织结构的牵拉,恢复视网膜的正常解剖位置的目的。便于手术后作清晰的眼底检查而有利于进行后续的光凝或冷凝等必需的治疗措施。
对糖尿病视网膜病变患者的视网膜脱离,应注意鉴别属牵拉性或孔源性。有些牵拉性视网膜脱离的患者,在不做手术治疗的情况下,较长时期尚能保存一定的视力,而孔源性脱离则必须早期手术治疗,否则在较短时间内大多视力丧失。对增殖性视网膜病变施行手术的目的在于缓解对视网膜或孔源性视网膜脱离的牵拉,可用玻璃体剪剪断厚的玻璃体增殖膜,还可对玻璃体新生血管施行眼内电凝,以及眼球环扎或巩膜折叠等手术使眼球内径减小。这些手术并可同时与闭合式玻璃体切割术联合进行。
由于发现体内
生长激素缺乏的侏儒糖尿病患者当中,很少发生糖尿病视网膜病变,曾经对糖尿病视网膜病变新生血管严重、光凝效果不佳的患者施行垂体部分切除手术,对部分患者减轻视网膜病变的血管病变有一定作用。可以减少出血水肿,导致新生血管萎缩,缓解血管病变。也可应用电凝和放射等方法破坏腺垂体,达到这些治疗目的。但这些疗法都必须慎用,对少数全身病情和视力预后较好,又不宜做光凝治疗的患者,可考虑选用。
3.光凝治疗 糖尿病视网膜病变后期,视网膜血管内外的病变引起视网膜严重缺血缺氧,因而导致血管增殖因子释放,刺激眼底的视盘和视网膜的新生血管形成。激光光凝视网膜组织使一定面积的神经视网膜组织破坏萎缩,降低患眼视网膜对氧的需求,以达到减少血管增殖因子的释放,从而缓解或清除视网膜缺血水肿和新生血管等病变的发生和发展。光凝治疗至今仍为对糖尿病视网膜病变的黄斑病变、新生血管出血等破坏视力严重后果的有效补救治疗方法。经激光光凝治疗,已有的新生血管可以消退,从而达到保持部分视网膜,尤其是黄斑区视网膜的视功能的目的。糖尿病视网膜病变的激光光凝治疗经近年大量的临床观察和多中心大规模的对照研究,已证明能够被眼底血红蛋白、黑色素、色素上皮较好吸收的氩绿激光,大面积视网膜光凝和直接对局部新生血管的封闭,以及对有渗漏性微血管瘤的凝固能起到很好的治疗作用。在非增殖性视网膜病变,光凝主要用于影响和对视力有严重威胁的黄斑病变患者,光凝针对成簇的微血管瘤与毛细血管闭塞的荧光渗漏区,也可用于近周边有广泛毛细血管闭塞而无黄斑病变的患者。由于光凝对需氧量高的外层视网膜灼伤成为瘢痕,视网膜变薄,可使内层从脉络膜血运得到较多氧的供应,并可消除由于缺氧而产生的血管增殖因子。光凝治疗前均须有完整清晰的眼底照相和荧光血管造影资料,详细了解病情和病变位置。
光凝对增殖性糖尿病视网膜病变在于针对新生血管防止出血,并阻止继续发生纤维组织。周边视网膜局限的新生血管可以采用全视网膜光凝,视盘新生血管,尤其对隆起的新生血管,也需进行弥散性光凝,或称全视网膜光凝,6~8周后未消退的新生血管可以在新生血管局部加密激光斑。所谓全视网膜光凝的光凝范围,为距视盘缘1个视盘直径至眼底赤道部,以及距黄斑中心上、下和颞侧各2个视盘直径,避开视盘黄斑束和颞侧上下血管弓之间的后极部视网膜,形成眼底一大片播散光凝点的椭圆形光凝区域。全视网膜光凝治疗虽为现在对重度糖尿病视网膜病变较好的疗法,但在术后有使视功能,包括夜间视力、颜色视力和周边视力减退的副作用,并常有中心视力轻度下降,患者还可发生自觉眼前闪光的症状。如术前已有黄斑水肿者,光凝术后有可能加重。此外,若术前已有严重的纤维血管增殖,术后有可能发生收缩而导致出血和视网膜脱离。光凝术后应注意必需的随诊观察,如发现有残余或复发新生血管,尚须作补充或重复的光凝治疗。
4.冷凝治疗 经裂隙灯显微镜和角膜接触镜进行的全视网膜激光光凝,不能到达视网膜前部,必要时可在眼球表面经眼前部结膜巩膜,或切开球结膜经巩膜作冷凝治疗,便可对视网膜周边部达到与光凝类似的治疗目的。另外,对眼有屈光间质混浊,如有白内障或玻璃体积血等,不能采用光凝的患者,需要时也用冷凝治疗。但因广泛的冷凝也可引起玻璃体收缩导致出血或视网膜脱离,对有重度玻璃体视网膜牵引的患者应慎用。



 流行病学
流行病学
 发病机制
发病机制
 临床表现
临床表现

 并发症
并发症
 实验室检查
实验室检查
 其他辅助检查
其他辅助检查
 鉴别诊断
鉴别诊断
 治疗
治疗
 预后
预后